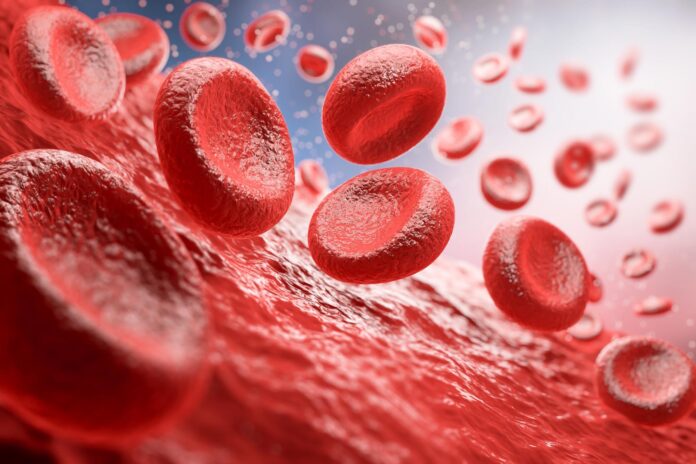
Durante décadas, una pregunta fundamental desconcertó a los hematólogos: ¿por qué dos personas con exactamente el mismo tipo de sangre poseen niveles muy diferentes de moléculas protectoras en sus glóbulos rojos?
Investigadores de la Universidad de Lund en Suecia finalmente han dado la respuesta. Al mirar más allá de los genes mismos y centrarse en cómo se “activan” y desactivan esos genes, los científicos han descubierto una capa oculta de regulación genética que podría revolucionar la seguridad de las transfusiones y nuestra comprensión de la resistencia a las enfermedades.
La capa oculta de la química de la sangre
Cuando hablamos de tipos de sangre, normalmente pensamos en las categorías estándar A, B, AB u O. Sin embargo, la compatibilidad sanguínea tiene muchos más matices. Depende de antígenos : moléculas específicas que se encuentran en la superficie de los glóbulos rojos y que actúan como tarjetas de identificación biológica.
El problema es que la cantidad de estos antígenos varía enormemente entre individuos.
“Si sólo tienes un par de cientos de moléculas de grupos sanguíneos por célula en lugar de mil o incluso un millón, existe el riesgo de que no se detecten en una prueba de compatibilidad, lo que puede afectar a la seguridad de una transfusión”, advierte Martin L. Olsson, profesor de Medicina de Transfusión en la Universidad de Lund.
Las pruebas de ADN estándar a menudo no logran detectar estas discrepancias porque observan el “modelo” (el gen) en lugar del “control de volumen” (la regulación).
El descubrimiento de los “interruptores” moleculares
Para resolver esto, el equipo de investigación cambió su enfoque de los genes a los factores de transcripción. Se trata de proteínas especializadas que actúan como interruptores moleculares; se unen a regiones específicas del ADN para determinar la cantidad de una proteína particular que produce una célula.
Utilizando un nuevo y sofisticado proceso computacional, el equipo mapeó casi 200 de estos sitios de unión en 33 genes de grupos sanguíneos diferentes. Esto les permitió identificar por qué ciertos genes, a pesar de estar presentes, apenas funcionaban.
Resolviendo el misterio de Helgeson
El avance proporcionó una respuesta a una anomalía médica legendaria conocida como grupo sanguíneo Helgeson. Descubierta en la década de 1970 por la tecnóloga médica Margaret Helgeson, esta rara variante se caracteriza por niveles extremadamente bajos de una proteína llamada Receptor del complemento 1 (CR1).
Durante cincuenta años, los científicos no pudieron encontrar la causa genética, ni siquiera analizando el propio ADN. El equipo de la Universidad de Lund descubrió que el problema no era un gen roto, sino un “interruptor” roto. Una pequeña mutación en el ADN impidió que el factor de transcripción necesario se uniera al gen. Como resultado, el gen simplemente “inactivo”, produciendo muchas menos moléculas de lo normal.
Una compensación evolutiva: protección versus riesgo
Este descubrimiento también destaca una fascinante intersección entre genética y evolución. El estudio encontró que esta variante específica de CR1 bajo es más común en las poblaciones tailandesas que en las suecas.
Hay una razón biológica para esto: los niveles más bajos de CR1 parecen brindar protección contra la malaria. Al dificultar que el parásito invada los glóbulos rojos, la mutación ofrece una ventaja de supervivencia en regiones donde la malaria es endémica. Esto ilustra un clásico equilibrio evolutivo, en el que un rasgo que complica los procedimientos médicos modernos puede haber sido un escudo vital contra enfermedades antiguas.
El futuro de la medicina transfusional
Las implicaciones de esta investigación se extienden mucho más allá de un solo grupo sanguíneo raro. El enfoque basado en datos del equipo ya está generando nuevos conocimientos:
- Diagnóstico mejorado: Los investigadores están trabajando para actualizar los chips de prueba basados en ADN para incluir estas variantes regulatorias recientemente descubiertas, lo que hace que la comparación de sangre sea significativamente más segura.
- Ampliando el mapa: Estudios de seguimiento ya han identificado problemas regulatorios similares en el crucial grupo sanguíneo RhD, lo que explica por qué algunos pacientes muestran niveles extremadamente bajos de la proteína a pesar de tener genes “normales”.
- Un nuevo modelo de investigación: Al combinar herramientas computacionales con datos epigenéticos, los científicos ahora pueden predecir cómo los diferentes grupos sanguíneos podrían afectar la susceptibilidad de una persona a diversas enfermedades.
Conclusión: Al cambiar el enfoque de las secuencias genéticas a la regulación genética, los científicos han salvado una brecha de 50 años en la ciencia de la sangre, allanando el camino para transfusiones más seguras y una comprensión más profunda de cómo nuestra biología nos protege de las infecciones.